Volumen 20 - Número 1 - Enero-Marzo 2012
Queratoplastia lamelar posterior (DSAEK)
P. Sauvageot, P. Pujol, J. Ãlvarez de Toledo
Centro de Oftalmología Barraquer
CORRESPONDENCIA
Paola Sauvageot
Centro de Oftalmología Barraquer
C/ Laforja, 83. 08021 Barcelona.
Email: psauvageot@barraquer.com
Centro de Oftalmología Barraquer
C/ Laforja, 83. 08021 Barcelona.
Email: psauvageot@barraquer.com
RESUMEN
La Descemet Stripping Automated Endotelial Keratoplasty (DSAEK) representa un significativo avance en términos de simplicidad quirúrgica, recuperación funcional, repetitividad y seguridad en aquellas patologías corneales causadas por una insuficiencia funcional del endotelio. La técnica de obtención del injerto donante es un paso crítico para conservar el recuento endotelial por lo que debe de ser segura y reproducible. A continuación describiremos la técnica de obtención del lentículo donante con microqueratomo que es la más utilizada en la actualidad. Tras colocar el botón corneo-escleral obtenido en una cámara anterior artifical, se procede a realizar el corte con el microqueratomo adecuando la velocidad de paso del mismo al espesor corneal con el fin de conseguir un lentículo posterior lo más fino posible. Durante las maniobras es importante evitar el colapso de la cámara anterior y el plegamiento de la córnea para evitar lesiones sobre la monocapa endotelial que comprometerían el pronóstico visual final.
RESUM
La Descemet Stripping Automated Endotelial Keratoplasty (DSAEK) representa un significatiu avenç en termes de simplicitat quirúrgica, recuperació funcional, repetitivitat i seguretat en aquelles patologies corneals causades per una insuficiència funcional de l’endoteli. La tècnica d’obtenció de l’empelt donant és un pas crític per conservar el recompte endotelial, motiu pel qual ha de ser segura i reproduïble. A continuació descriurem la tècnica d’obtenció de l’empelt donant amb microqueràtom, que és la més utilitzada actualment. Després de col•locar el botó còrnio-escleral a una càmara anterior artificial, es procedeix a realitzar el tall amb el microqueràtom adecuant la velocitat de pas d’aquest a l’espessor corneal per tal d’aconseguir un empelt posterior tan fi com sigui possible. Durant les maniobres és important evitar el col•lapse de la càmera anterior i el plegament de la còrnia per evitar lesions a la monocapa endotelial que podrien comprometre el pronòstic visual final.
ABSTRACT
Descemet Stripping Automated Endotelial Keratoplasty (DSAEK) represents a significant advance in terms of surgical simplicity, functional recovery, repeatability and safety in those diseases caused by corneal endothelial disfunction. The technique of obtaining the donor graft is a critical step to preserve the endothelial count so it must be safe and reproducible. We will describe the technique of obtaining the donor lenticule using a microkeratome. After placing the corneo-scleral button in an artificial anterior chamber, we proceed to make the cut with the microkeratome adjusting the cutting speed to the corneal thickness in order to get a posterior lenticule as thin as possible. During the maneuvers it is important to avoid the collapse of the anterior chamber and the folding of the cornea to prevent injury on the endothelial monolayer that would compromise the final visual prognosis.
Introducción
La queratoplasita lamelar posterior se emplea en la actualidad como tratamiento quirúrgico de aquellas patologías corneales congénitas o adquiridas (distrofia endotelial de Fuchs, distrofia polimorfa posterior, queratopatías bullosas post-quirúrgicas) en las que la afectación corneal esté causada por una insuficiencia funcional de la monocapa celular endotelial. La sustitución quirúrgica de la misma por un endotelio sano resuelve el edema estromal y epitelial sin eliminar el estroma del receptor, tal y como se realiza en la queratoplastia penetrante. Esta técnica representa un significativo avance en términos de simplicidad quirúrgica, recuperación funcional, repetitividad y seguridad.
Técnica quirúrgica
A continuación describimos la técnica quirúrgica que empleamos en nuestro Centro. La técnica de obtención del lentículo donante con microqueratomo es la más utilizada en la actualidad. El botón corneo-escleral se coloca en la cámara anterior artificial (ALTK, Moria) para mantener una adecuada presión durante el paso del microqueratomo. Trabajamos con un botón corneo-escleral de un diámetro de 17 mm. para conseguir una perfecta fijación y presurización durante el corte. Comprobamos el centrado con el anillo de fijación para evitar descentramientos del corte lamelar, medimos la presión con el tonómetro de Barraquer y el espesor corneal inicial con un paquímetro ultrasónico. En general se recomienda eliminar todo el epitelio corneal antes del corte para evitar la posibilidad de implantar células epiteliales en la entrecara donante-receptor y reducir el espesor corneal inicial en unas 50-70 μ.Procedemos a realizar el corte con el microqueratomo con un cabezal de 350 micras adecuando la velocidad de desplazamiento del microqueratomo (a menor velocidad de paso, mayor profundidad de corte) al espesor corneal donante (Figura 1).
Comprobamos la regularidad y diámetro del mismo, realizamos una nueva medición paquimétrica que nos informa del espesor final del donante obtenido y colocamos el flap anterior de nuevo sobre el botón corneo-escleral. Procedemos al secado de los bordes de corte y esperamos unos instantes hasta comprobar su buena adherencia. Posteriormente, marcamos con rotulador quirúrgico los bordes de corte para que, cuando invirtamos la córnea al colocarla sobre la base de trepanación, realicemos un correcto centrado de la misma.
Figura 1. Cámara artifical ALTK de Moria. Corte del lentículo posterior con microqueratomo.
Tras realizar el corte debemos retirar el botón de la cámara anterior artificial para proceder a su trepanación sobre una base curva de teflón. Durante esta maniobra es importante evitar el colapso de la cámara anterior y el plegamiento de la córnea para evitar lesiones sobre la monocapa endotelial. Para ello, mantenemos la infusión abierta y retiramos paulatinamente la rosca de fijación, siempre manteniendo la perfusión en el interior de la cámara. Podemos también invertir la misma colocando la córnea mirando hacia el suelo, para que, al cerrar la infusión, el peso del líquido nos mantenga la cornea en su forma anatómica sin colapsarla. Una vez separada la rosca, retiramos el botón corneo-escleral y lo colocamos, o bien en un frasco con medio de preservación si no lo empleamos inmediatamente, o sobre una base de un trépano de punch si lo vamos a utilizar a continuación.
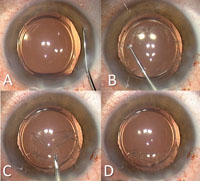
En el paciente realizamos inicialmente dos paracentesis a las 2 y a las 10 horas y una incisión superior de 2.8 mm. que luego ampliaremos a 4.1 mm antes de la inserción del donante. Inyectaremos aire o viscoelástico cohesivo según el caso para mantener la cámara anterior. Procedemos a realizar la descemetorrhexis mediante un gancho de Sinskey inverso (K3-5002, Katena Products, Inc., Denville NJ, EE.UU.) con el que realizamos un desgarro periférico en los 360º. Con una espátula recogemos el endotelio centrípetamente y, con una pinza de John (AE-4962, Asico LLC, Westmont, IL), lo extraemos finalmente de las 6h a las 12h (Figura 2). Retiramos meticulosamente el viscoelástico, en caso de haberlo utilizado, con cánulas de irrigación-aspiración.
Figura 2. Descemetorrhexis. A. Realizamos un desgrro periférico circular en los 360º. B. Con una espátula recogemos el endotelio centrípetamente. C, D.Con una pinza de John extraemos finalmente el endotelio de las 6 a las 12 horas.
A continuación, trepanamos el botón donante. Mediante las marcas realizadas previamente centramos el botón en la base del trépano y lo cortamos con un trépano de punch de Hessburg-Barron. Antes de cortar siempre comprobamos a través del orificio central del trépano que estamos por dentro de las marcas superficiales del corte lamelar anterior en los 360º.
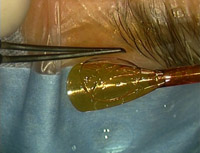
Colocamos el lentículo obtenido sobre el lecho del inyector EndoSaver (Ocular Systems, Inc.Winston-Salem, NC) con el endotelio hacia arriba y descentrado para facilitar el correcto plegamiento del mismo (Figura 3). Enroscamos lentamente el inyector quedando el lentículo enrollado con la cara estromal hacia afuera (Figura 4). Rotamos el inyector 180º de manera que la cara endotelial quede hacia abajo al inyectarse. La irrigación incorporada al inyector permite controlar la profundidad de la cámara anterior sin necesidad de mantenedor de cámara y evita así descompresiones que comprometerían la integridad endotelial del botón donante durante la inyección del mismo. En la cirugía de DSAEK la pérdida celular descrita oscila entre un 9 y un 35 %1-3 dependiendo de las técnicas de inserción empleadas.
Figura 3. Colocamos el lentículo posterior sobre la pala del inyector EndoSaver.
Figura 4. Enroscamos lentamente el inyector quedando el lentículo enrollado con la cara estromal hacia afuera.
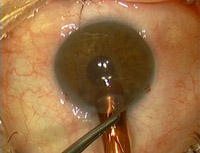
Una vez el donante se ha desplegado correctamente en la cámara anterior (Figura 5) procedemos a inyectar una burbuja de aire que, ocupando toda la cámara anterior, lo adhiera a la cara posterior de la córnea receptora. Tras comprobar que el disco está centrado, con una cánula realizamos movimientos de compresión centrífugos sobre la superficie corneal para drenar el líquido que pudiera quedar en la entrecara. Se debe intentar conseguir una cierta presión en el globo para facilitar su adhesión.
Figura 5. Desplegamos el lentículo endotelial en la cámara anterior y a continuación inyectamos una burbuja de aire para adherirlo al estroma receptor.
Mantenemos al paciente en decúbito supino durante unos 10 minutos en la camilla de quirófano. Después de este tiempo, lavamos con BSS la cámara anterior dejando una burbuja de aire que ocupe entorno al 40% de la cámara anterior para evitar un bloqueo pupilar en el postoperatorio. No realizamos iridectomía periférica. Hidratamos las paracentesis intentando conseguir una perfecta hermeticidad. El paciente permanece posteriormente en decúbito supino sin almohada en su cama durante unas horas para intentar evitar la dislocación del disco.
Discusión
Los avances técnicos y quirúrgicos desarrollados en la última década han facilitado el resurgir de la cirugía lamelar posterior y estamos asistiendo a un avance vertiginoso de conocimientos, técnicas y resultados en este campo. Se ha convertido en el procedimiento de elección para numerosos cirujanos en el tratamiento de las distrofias endoteliales y descompensaciones corneales secundarias4,5.Estas técnicas han supuesto un avance en la recuperación de los pacientes y en una rápida rehabilitación visual6, aunque no están exentas de complicaciones. La recuperación de la agudeza visual potencial máxima puede verse comprometida en algunos casos por la presencia de alteraciones en la interfase entre el estroma del donante y el estroma del receptor, hallazgos que se observan con los estudios de microscopía confocal7.
Bajo el punto de vista de la agudeza visual final, la cirugía ideal8,9 sería el reemplazo quirúrgico aislado del endotelio lesionado (DMEK) ya que no existe interfase donante receptor susceptible de limitar la recuperación visual. Esta técnica se está ya perfilando como reemplazo a la cirugía de DSAEK en aquellos casos en los que la visualización de la cámara anterior permita su realización con seguridad. Probablemente en pocos años el vertiginoso desarrollo de mejores instrumentos, maniobras quirúrgicas y nuevos conceptos en la fisiología del endotelio trasplantado modifique el panorama quirúrgico actual.
Bibliografía
-
Chen ES, Terry MA, Shamie N, Hoar KL, Phillips PM, Friend DJ. Endothelial Keratoplasty: Vision, Endothelial Survival, and Complications in a Comparative Case Series of Fellows vs Attending Surgeons. Am J Ophthalmol. 2009 Apr 15. Epub ahead of print.
- Mehta JS, Por YM, Poh R, Beuerman RW, Tan D. Comparison of donor insertion techniques for descemet stripping automated endothelial keratoplasty. Arch Ophthalmol. 2008 Oct;126(10):1383-8
- Busin M, Bhatt PR, Scorcia V. A modified technique for descemet membrane stripping automated endothelial keratoplasty to minimize endothelial cell loss. Arch Ophthalmol. 2008 Aug;126(8):1133-7.
- Bronner A. Descemet's stripping automated endothelial keratoplasty. Optom Vis Sci. 2008 Sep;85(9):E808-13.
- Bachmann BO, Pogorelov P, Kruse FE, Cursiefen C. Patient satisfaction after posterior lamellar keratoplasty (DSAEK) Klin Monatsbl Augenheilkd. 2008 Jun;225(6):577-81
- Price MO, Price FW. Descemet’s stripping endothelial keratoplasty. Curr Opinion Ophthalmol 2007 Jul; 18(4):290-4
- Kobayashi A, Mawatari Y, Yokogawa H, Sugiyama K. In vivo laser confocal microscopy after descemet stripping with automated endothelial keratoplasty. Am J Ophthalmol. 2008 Jun;145(6):977-985.
- Dapena I, Ham L, Melles GR Endothelial keratoplasty: DSEK/DSAEK or DMEK: the thinner the better? Curr Opin Ophthalmol. 2009 May 4 Epub ahead of print.
- Ham L, Balachandran C, Verschoor CA, van der Wees J, Melles GR. Visual rehabilitation rate after isolated descemet membrane transplantation: descemet membrane endothelial keratoplasty. Arch Ophthalmol. 2009 Mar;127(3):252-5